Curso de Fisiología

EQUILIBRIO IONICO Y POTENCIAL DE MEMBRANA
 |
POTENCIAL ELECTROQUIMICO DE LOS IONES(*) Una membrana separa dos soluciones acuosas en dos compartimentos A y B. El ión X+ se encuentra más concentrado del lado A que del B. Si no hay una diferencia de potencial entre ambos lados de la membrana, X+ tenderá a ir de A a B lo mismo que si se tratara de una partícula no cargada. Si se aumenta la concentración del ión X+ en el lado A, los iones tenderán a emigrar hacia B llevándose consigo su carga eléctrica creando una diferencia de potencial. Se alcanza el equlibrio electroquímico cuando la carga + del compatimento B aumenta de tal modo que repele más iones positivos. Este equilibrio se debe a que:
El potencial eléctrico que se alcanza en el equilibrio viene dado por la ecuación de Nernst:
Para un sistema hipotético simple, la ecuación de Nernst permite predecir exactamente el potencial eléctrico a través de una memebrana. Si por ejemplo, la concentración de K+ es de 100 mM en lado y de 1 mM en el lado B, el potencial de membrana será de - 116 mV. Es decir, la ecuación de Nernts es lineal cuando se representa el potencial de membrana frente al logarítmo del conciente de concentraciones (*) Sin embargo, en los sistemas biológicos la situación es más compleja: suelen coexistir diferentes tipos de iones, de tamaños y cargas diferentes y, algunas proteínas cargadas pueden también influir sobre el potencial de membrana |
|||
 |
Consideremos un sistema en el que una membrana separa dos compartimentos en los que existen diferentes concentraciones de Na+ y de K+ (por ejemplo KCl 10 mM + NaCl 1 mM en el compartimento de la izquierda KCl 1 mM + NaCl 10 mM en de la derecha)(*). Si la membrana solo es permeable al K, al ser más concentrada la solución de la izquierda habrá un migración de los K+ hacia la derecha quedándose el compartimento de la izquierda con carga negativa. Si la membrana es sólo permeable al Na+, ocurre la situación inversa. Al ser más concentrada en NaCl la solución de la derecha habrá un desplazamiento de carga hacia el compartimento de la izquierda. Dado que en la realidad las membranas no son totalmente impermeables, Goldman modificó la ecuación de Nernst en 1943 para tener en cuenta la participación de los iones más importantes implicados en la membrana de las neuronas.
A medida que la membrana se despolariza (por llegada de una señal sináptica, por ejemplo), se hace permeable al Na+ cuya concentración en el exterior de la neurona es muy superior a la del interior. En consecuencia hay una entrada masiva de sodio a través de la membrana con lo que se produce el potencial de acción. Este es de corta duración ya que inmediatamente se restablece la permeabilidad de la membrana al K+, con lo que el potencial de la membrana vuelve a su posición de reposo. |
|||
|
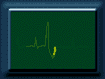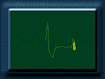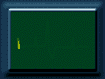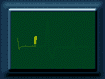
BASE IONICA DE LOS POTENCIALES DE ACCION La acción de las bombas iónicas crea gradientes transmembrana sustancias para la mayoría de los iones (*). Una vez conocidos estos valores, la ecuación de Goldman o incluso la de Nernst permiten calcular los potenciales de reposo que son negativos en casi todas las células. Como hemos visto, el cambio de permeabilidad del Na es el responsable de la generación de un potencial de acción. La pregunta que hay que formular, es ¿porqué se produce este cambio? Para contestar a esta pregunta, Katz y Hodkin estudiaron como afectaba la concentración de sodio el potencial de acción en la membrana del axón del calamar gigante. Estos autores observaron que la reducción de la concentración de Na+ reducía tanto el ritmo de elevación del potencial de acción como su amplitud pico (*) . Además, encontraron una relación casi lineal entre la amplitud del potencial de acción y el logaritmo de la concentración, lo que era de esperar según la ecuación de Nernst asumiendo que la membrana axolémica es selectivamente permeable para el sodio. Por el contrario, el potencial de reposo se mantenía prácticamente constante al variar la concentración de sodio. Por lo tanto, aunque en reposo la membrana de la neurona es sólo ligeramente permeable al sodio, se torna extraordinariamente permeable a este ión durante las fases de ascenso y sobrepico del potencial de acción. Este aumento de la permeabilidad se debe a la apertura de unos canales selectivos para sodio para sodio, que están cerrados en condiciones de reposo. Como la concentración extracelular de sodio es superior a la intracelular (*), al abrirse el canal hay un flujo de iones hacia el interior de la célula con lo que la membrana se despolariza y se aproxima al valor de + 60 mV. El tiempo durante el cual la membrana se mantiene despolarizada es muy breve (del orden de milisegundos). Inmediatamente la membrana se repolariza pasando por una fase de hiperpolarización transitoria. Como se verá, esto es debido a que se produce momentáneamente un aumento de la permeabilidad al potasio. LAS CORRIENTES IÓNICAS A TRAVÉS DE LAS MEMBRANAS La clave para comprender para comprender porque se inicia el potencial de acción cuando hay un incremento transitorio de la membrana al Na+ es la observación de que estos sólo se desarrollan cuando el potencial de la membrana sobrepasa un valor umbral.
Utilizando el método de control de voltaje, Hodgkin y Huxley hicieron las siguientes obervaciones:(*) |
|||
|
La sensibilidad al voltage de la corriente temprana (es decir porqué tiene forma de U cuando el potencial de membrana pasa de -68 mV a 0 mV, aumentando, pasando por un máximo y anulándose finalmente) permite deducir la naturaleza de los iones. En efecto, los primeros experimentos de Hodgkin y Huxley fueron realizados con concentraciones de sodio de 440 mM en el exterior de la neurona y de 50 mM en el interior. Para estas concentraciones, la aplicación de la ecuación de Nernst predice un potencial de equilibrio de -55 mV. Por lo tanto, la observación experimental de que a + 52 mV no hay corriente temprana, indica que esta corriente de ingreso de cargas positivas al interior es debida a sodio. Si se elimina el Na+ externo, el exterior del axón se torna negativo. En estas condiciones si se aumenta la permeabilidad de la membrana al sodio, este deberá fluir desde dentro hacia afuera debido al gradiente de concentración invertido. Y, efectivamente, cuando Hodgkin y Huxley hicieron el experimento observaron que la corriente temprana invertía su polaridad. Por el contrario, la eliminación de Na+ del exterior tiene poca influencia sobre la corriente tardía que tiene lugar cuando se ha despolarizado la membrana, lo que indica que debe ser debida a un ión diferente del Na+. Pronto se demostró, empleando entre otros elementos potasio radioactivo que la corriente tardía era debida al una migración del potasio de adentro a afuera. En conclusión, el potencial de acción se debe a la acción conjunta de dos corrientes iónicas: una corriente temprana de sodio, de afuera hacia adentro, de corta duración, seguida de una corriente de potasio, de dentro a afuera más sostenida. Desde los experimentos de Hodgkin y Huxley, son numerosas las pruebas que se han encontrado de que existen dos mecanismos que regulan las corrientes iónicas en las neuronas. Una de ellas es la utilización de los agentes farmacológicos que afectan selectivamente estas dos corrientes:
|